Одавно је познато да сви молекули поседују два једнака и супротна набоја која су раздвојена на одређеној удаљености. У случају таквих поларних молекула, центар негативног наелектрисања се не подудара са центром позитивног набоја. Степен поларности у таквим ковалентним молекулама може се описати термином Диполе Момент, који је у суштини мера поларности у поларној ковалентној вези.
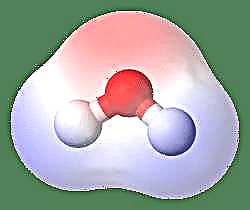
Најједноставнији пример дипола је молекул воде. Молекула воде је поларна због неједнаког дељења својих електрона у „савијеној“ структури. Молекул воде формира угао, са атомима водоника на врховима и кисеоником у врху. Пошто кисеоник има већу електронегативност од водоника, страна молекула са атомом кисеоника има делимични негативни набој док водоник, у центру, има делимични позитивни набој. Због тога смјер диполног момента показује према кисеонику.
На језику физике, електрични диполни момент је мера одвајања позитивних и негативних електричних наелектрисања у систему наелектрисања, односно мерило укупне поларности система наелектрисања - тј. Одвајање електричног набоја молекула, који доводи до дипола. Математички, у једноставном случају два тачкаста наелектрисања, једног са набојем + к и једног са набојем? К, електрични диполни момент п може се изразити као: п = кд, где је д вектор помака који показује од негативног наелектрисања до позитивно наелектрисање. Дакле, вектор електричног диполног момента п показује од негативног на позитивног набоја.
Други начин да га погледамо је представљање Диполовог момента грчким словом м, м = ед, где је е електрични набој и д је удаљеност раздвајања. Изражава се у јединицама Дебие и пише се као Д (где је 1 Дебие = 1 к 10-18е.с.у цм). Диполни момент је векторска количина и зато је представљена малом стрелицом с репом у позитивном центру и главом која је окренута према негативном центру. У случају молекуле воде, момент дипола је 1,85 Д, док је молекул хлороводоничне киселине 1,03 Д и може се представити као:
Написали смо много чланака о диполском тренутку за Спаце Магазине. Ево чланка о чему се прави вода и ево чланка о молекулама.
Ако желите више информација о тренутку дипола, погледајте ове чланке из часописа Хиперпхисицс анд Сциенце Даили.
Такође смо снимили читаву епизоду Астрономске глуме о молекулама у свемиру. Слушајте овде, епизода 116: Молекуле у свемиру.
Извори:
хттп://ен.википедиа.орг/вики/Елецтриц_диполе_момент
хттп://ен.википедиа.орг/вики/Диполе
хттп://ввв.туторвиста.цом/цонтент/цхемистри/цхемистри-иии/цхемицал-бондинг/дегрее-поларити.пхп
хттп://хиперпхисицс.пхи-астр.гсу.еду/хбасе/елецтриц/диполе.хтмл#ц1
хттп://ен.википедиа.орг/вики/Ватер_молецуле